人教版(2019)化学必修第二册《氮及其化合物》化工生产中的重要非金属元素PPT课件(第2课时氨和铵盐)
展开
《氮及其化合物》化工生产中的重要非金属元素PPT课件(第2课时氨和铵盐)
第一部分内容:核心素养发展目标
1.能从物质类别、氮元素价态的角度,认识氨、铵盐的性质与转化,促进“证据推理与模型认知”化学核心素养的发展。
2.设计实验,如氨的性质实验、制备实验,铵盐的性质实验及铵离子的检验等,实现氨的转化与生成,增强“科学探究”意识。
... ... ...
氮及其化合物PPT,第二部分内容:01氨的性质
知识梳理
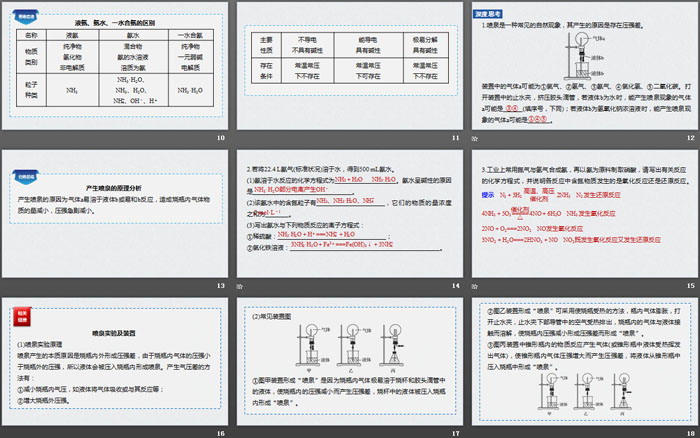
1.氨的物理性质
氨是一种无色有__________气味的气体,密度比空气_______,容易_______。
2.氨极易溶于水且与水反应
(1)喷泉实验
①按图所示装置,打开止水夹,挤压滴管的胶头,烧杯中的溶液由玻璃管进入烧瓶,形成_______,烧瓶内液体呈_______色。
②上述实验说明氨_______于水,其水溶液呈_______性。
(2)氨与水的反应
①氨气易与水反应:_____________________,其水溶液称为氨水。在氨水中:_____________________,氨水具有_______性,能使石蕊溶液变蓝。
②氨水中的氮元素主要以______________的形式存在,只有少量的NH3·H2O电离为NH 和OH-,但在求氨水的物质的量浓度、质量分数时应将_______视为溶质。
③NH3·H2O不稳定,受热易分解:____________________________,因此,氨水应密封保存在阴凉处。
3.氨与酸反应
(1)氨与氯化氢相遇时的现象是____________,反应的化学方程式是________________________。
(2)工业上用氨、二氧化碳和水制取碳酸氢铵的化学方程式是____________________________________ 。
(3)工业上用硫酸吸收氨的化学方程式是____________________________________。
4.氨具有还原性
(1)请写出氨气与氧气在催化剂作用下生成NO的化学方程式:____________________________________。
(2)氨气可被氧化铜氧化为氮气,反应的化学方程式为____________________________________ 。
判断正误
(1)液氨可用作制冷剂,是因为其汽化时吸收大量的热( )
(2)氨水能导电,所以氨水是电解质( )
(3)新制饱和氨水中含氮粒子物质的量浓度最大的是NH ( )
(4)将蘸有浓氨水的玻璃棒靠近浓硫酸有白烟产生( )
(5)氨中氮元素的化合价为-3价,在反应中只能升高而具有还原性( )
深度思考
1.喷泉是一种常见的自然现象,其产生的原因是存在压强差。
装置中的气体a可能为①氯气、②氢气、③氨气、④氯化氢、⑤二氧化碳。打开装置中的止水夹,挤压胶头滴管,若液体b为水时,能产生喷泉现象的气体a可能是_______ (填序号,下同);若液体b为氢氧化钠浓溶液时,能产生喷泉现象的气体a可能是_______。
归纳总结
产生喷泉的原理分析
产生喷泉的原因为气体a易溶于液体b或易和b反应,造成烧瓶内气体物质的量减小,压强急剧减小。
2.若将22.4 L氨气(标准状况)溶于水,得到500 mL氨水。
(1)氨溶于水反应的化学方程式为_____________________。氨水呈碱性的原因是_____________________。
(2)该氨水中的含氮粒子有_____________________,它们的物质的量浓度之和为_______ 。
(3)写出氨水与下列物质反应的离子方程式:
①稀硫酸:__________________________________________;
②氯化铁溶液:__________________________________________。
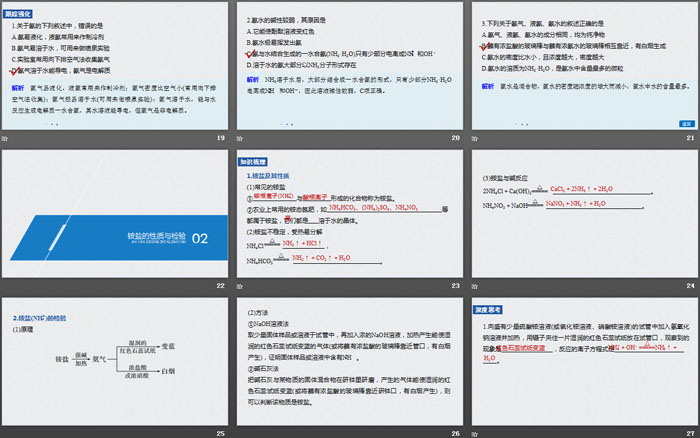
3.工业上常用氮气与氢气合成氨,再以氨为原料制取硝酸,请写出有关反应的化学方程式,并说明各反应中含氮物质发生的是氧化反应还是还原反应。
相关链接
喷泉实验及装置
(1)喷泉实验原理
喷泉产生的本质原因是烧瓶内外形成压强差,由于烧瓶内气体的压强小于烧瓶外的压强,所以液体会被压入烧瓶内形成喷泉。产生气压差的方法有:
①减小烧瓶内气压,如液体将气体吸收或与其反应等;
②增大烧瓶外压强。
(2)常见装置图
①图甲装置形成“喷泉”是因为烧瓶内气体极易溶于烧杯和胶头滴管中的液体,使烧瓶内的压强减小而产生压强差,烧杯中的液体被压入烧瓶内形成“喷泉”。
②图乙装置形成“喷泉”可采用使烧瓶受热的方法,瓶内气体膨胀,打开止水夹,止水夹下部导管中的空气受热排出,烧瓶内的气体与液体接触而溶解,使烧瓶内压强减小形成压强差而形成“喷泉”。
③图丙装置中锥形瓶内的物质反应产生气体(或锥形瓶中液体受热挥发出气体),使锥形瓶内气体压强增大而产生压强差,将液体从锥形瓶中压入烧瓶中形成“喷泉”。
跟踪强化
1.关于氨的下列叙述中,错误的是
A.氨易液化,液氨常用来作制冷剂
B.氨气易溶于水,可用来做喷泉实验
C.实验室常用向下排空气法收集氨气
D.氨气溶于水能导电,氨气是电解质
2.氨水的碱性较弱,其原因是
A.它能使酚酞溶液变红色
B.氨水极易挥发出氨
C.氨与水结合生成的一水合氨(NH3·H2O)只有少部分电离成NH 和OH-
D.溶于水的氨大部分以NH3分子形式存在
3.下列关于氨气、液氨、氨水的叙述正确的是
A.氨气、液氨、氨水的成分相同,均为纯净物
B.蘸有浓盐酸的玻璃棒与蘸有浓氨水的玻璃棒相互靠近,有白烟生成
C.氨水的密度比水小,且浓度越大,密度越大
D.氨水的溶质为NH3·H2O,是氨水中含量最多的微粒
... ... ...
氮及其化合物PPT,第三部分内容:02铵盐的性质与检验
知识梳理
1.铵盐及其性质
(1)常见的铵盐
①_______________与_______________形成的化合物称为铵盐。
②农业上常用的铵态氮肥,如______________________________等都属于铵盐,它们都是 溶于水的晶体。
(2)铵盐不稳定,受热易分解
NH4Cl ______________________________,
NH4HCO3 ______________________________。
(3)铵盐与碱反应
2NH4Cl+Ca(OH)2 ______________________________ 。
NH4NO3+NaOH ______________________________。
2.铵盐(NH )的检验
(1)原理
(2)方法
①NaOH溶液法
取少量固体样品或溶液于试管中,再加入浓的NaOH溶液,加热产生能使湿润的红色石蕊试纸变蓝的气体(或将蘸有浓盐酸的玻璃棒靠近管口,有白烟产生),证明固体样品或溶液中含有NH 。
②碱石灰法
把碱石灰与某物质的固体混合物在研钵里研磨,产生的气体能使湿润的红色石蕊试纸变蓝(或将蘸有浓盐酸的玻璃棒靠近研钵口,有白烟产生),则可以判断该物质是铵盐。
深度思考
1.向盛有少量硫酸铵溶液(或氯化铵溶液、硝酸铵溶液)的试管中加入氢氧化钠溶液并加热,用镊子夹住一片湿润的红色石蕊试纸放在试管口,观察到的现象是__________________,反应的离子方程式是__________________。
2.铵盐溶液与碱溶液反应的离子方程式
(1)铵盐溶液与烧碱溶液混合后加热:__________________。
(2)铵盐稀溶液与烧碱稀溶液混合:__________________。
(3)铵盐浓溶液与烧碱浓溶液混合:__________________。
3.根据铵盐的性质,分析应当怎样合理地储存和施用铵态氮肥?
提示 贮存铵态氮肥时,为了防止受热分解,应密封包装并放在阴凉通风处;施肥时应将铵态氮肥埋在土下,且不能与碱性物质(如草木灰)混用。
特别提示
(1)铵盐受热分解都有氨生成,但硝酸铵受热分解最终生成氮气或氮氧化物。
(2)分别用试管加热氯化铵和单质碘时,都由固体变为气体,而在试管口遇冷又凝结为固体,其本质不同,前者为化学变化,后者为物理变化。
(3)检验溶液中含有NH 时,需要加入浓碱溶液并加热,其目的是利用氨气的生成与检验。
跟踪强化
1.下列关于铵盐的说法中正确的是
A.所有铵盐受热均可以分解,其产物中都有氨
B.所有铵盐都易溶于水,所有铵盐中的N均呈-3价
C.氯化铵溶液中加入烧碱浓溶液共热时反应的离子方程式为NH +OH-===NH3↑+H2O
D.氯化铵和氯化钠的固体混合物可用升华法分离
... ... ...
氮及其化合物PPT,第四部分内容:03氨的实验室制法
知识梳理
实验室制取氨的实验装置如图所示:
(1)反应原理:______________________________。
(2)碱石灰的作用:__________________________ 。
(3)由于氨极易溶于水,不能用排水法收集,常用______________法来收集。
(4)验满方法
①把湿润的红色石蕊试纸置于试管口,试纸变_________;
②将蘸有浓盐酸的玻璃棒置于试管口,有_________产生。
(5)尾气处理
可在导管口放一团用__________________浸湿的棉花球。
深度思考
1.制取氨气的发生装置与实验室制取哪种气体的相同?使用该装置需注意什么问题?
提示 与实验室制取氧气的发生装置相同。该套装置在使用时要特别注意加热时要使试管口略低于管底,以防止冷凝水倒流使试管炸裂。
2.在制取氨的实验装置中,使用棉花的作用是什么?
提示 若为干燥的棉花则起到减缓氨气与空气对流的作用;若为蘸有水或稀硫酸的棉花,则还可以吸收多余的NH3。
3.氨气是化学实验室常需制取的气体。实验室制取氨气通常有两种方法:
①用固体氢氧化钙与氯化铵共热反应;
②在常温下用固体氢氧化钠与浓氨水混合反应。
(1)下面的发生装置图中,方法①应选用装置_______(填“A”或“B”,下同),方法②应选用装置______。
(2)在制取氨气后,如果要干燥氨气,应选用的干燥剂是______(填字母)。
A.浓硫酸 B.固体氢氧化钠
C.五氧化二磷 D.稀硫酸
(3)如图是收集氨气的几种装置,其中可行的是________,集气的原理是__________________________。
特别提示
(1)制取氨时,不能用硝酸铵代替氯化铵。因为硝酸铵在加热过程中可能发生爆炸性的反应,发生危险。
(2)制取氨时,不能用氢氧化钠代替熟石灰。因为氢氧化钠具有吸湿性,易结块,不利于产生NH3,且在加热条件下易腐蚀试管。
(3)氨气是碱性气体,不能用酸性干燥剂(浓硫酸等)干燥,也不能用无水CaCl2干燥,因为它们均能与氨气发生反应,常用碱石灰作干燥剂。
跟踪强化
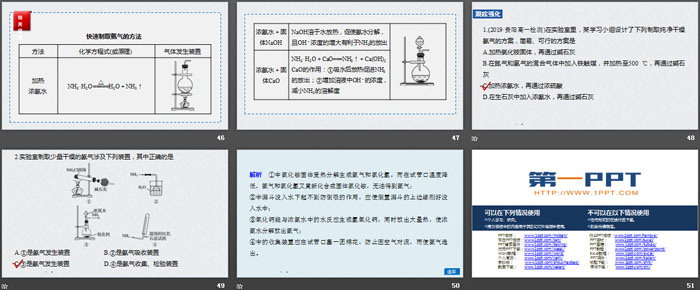
1.(2019·贵阳高一检测)在实验室里,某学习小组设计了下列制取纯净干燥氨气的方案,简易、可行的方案是
A.加热氯化铵固体,再通过碱石灰
B.在氮气和氢气的混合气体中加入铁触媒,并加热至500 ℃,再通过碱石灰
C.加热浓氨水,再通过浓硫酸
D.在生石灰中加入浓氨水,再通过碱石灰
2.实验室制取少量干燥的氨气涉及下列装置,其中正确的是
A.①是氨气发生装置 B.②是氨气吸收装置
C.③是氨气发生装置 D.④是氨气收集、检验装置
... ... ...
关键词:人教版高中化学必修二PPT课件免费下载,化工生产中的重要非金属元素PPT下载,氮及其化合物PPT下载,氨和铵盐PPT下载,.PPT格式;